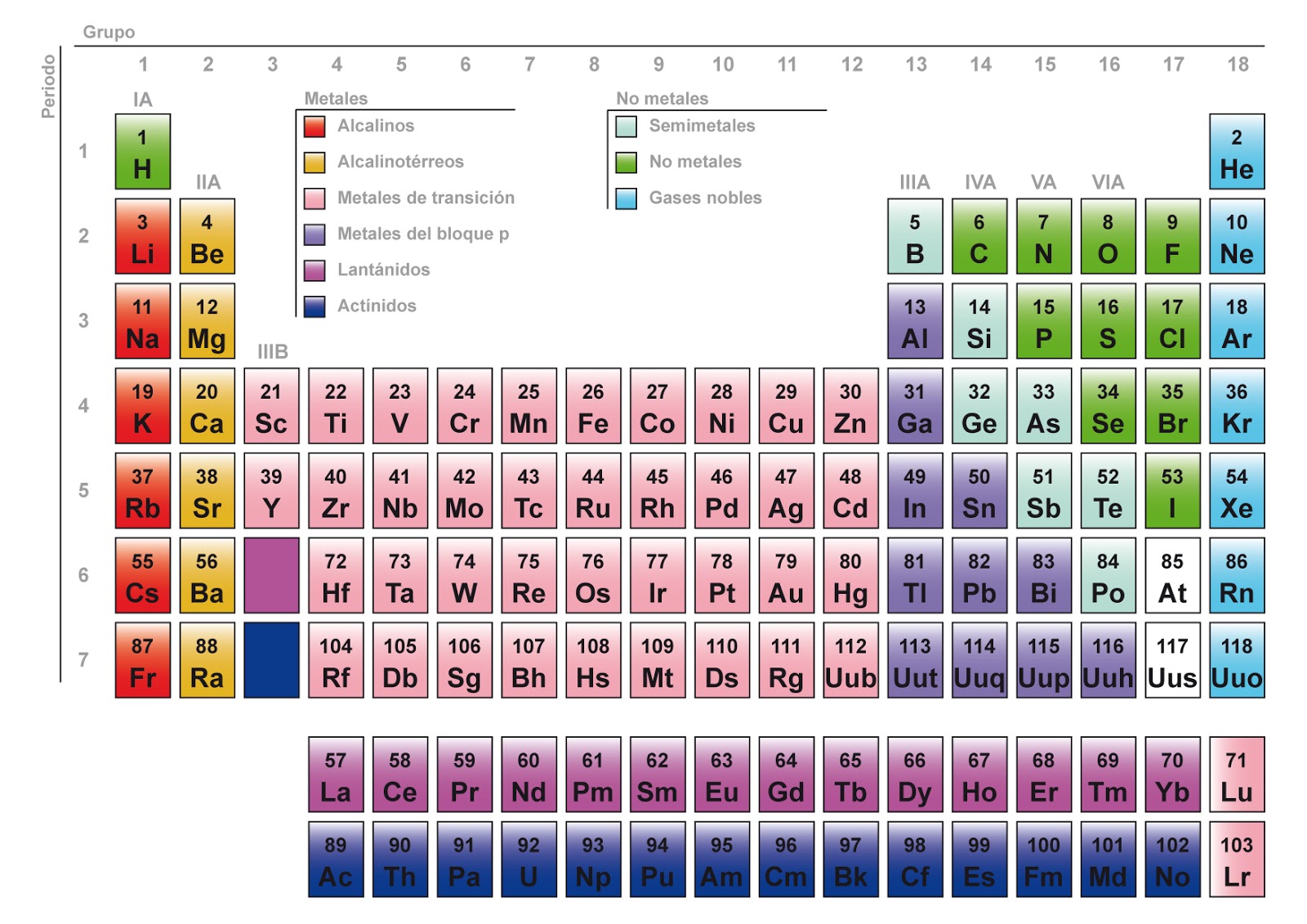
Cuales Son Sus Elementos Y Como Se Relacionan
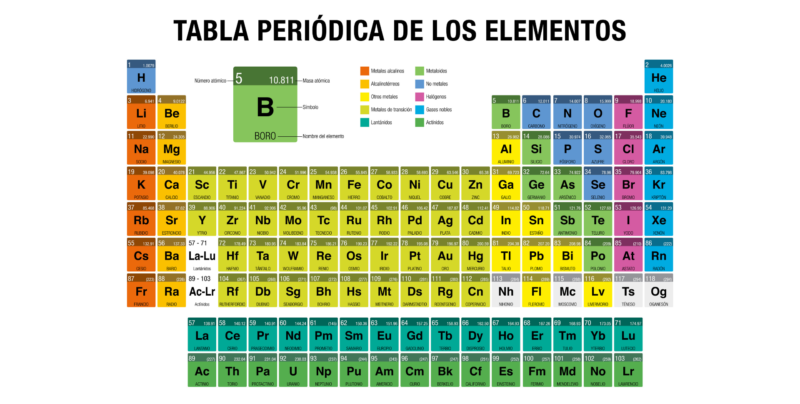
Al enseñar sobre los elementos y sus relaciones, es crucial comenzar con una base sólida. Asegurémonos de que los estudiantes comprendan qué constituye un elemento. Simplifiquemos la definición: un elemento es una sustancia pura que no se puede descomponer en sustancias más simples por medios químicos ordinarios. Cada elemento está definido por su número atómico, que representa el número de protones en su núcleo.
Explicar los elementos de forma accesible es fundamental. Utiliza ejemplos cotidianos. El oxígeno que respiramos es un elemento. El hierro en herramientas y estructuras también lo es. El oro en la joyería es otro ejemplo. Hacer referencia a ejemplos familiares ayuda a concretar la idea.
La Tabla Periódica: Un Mapa de los Elementos
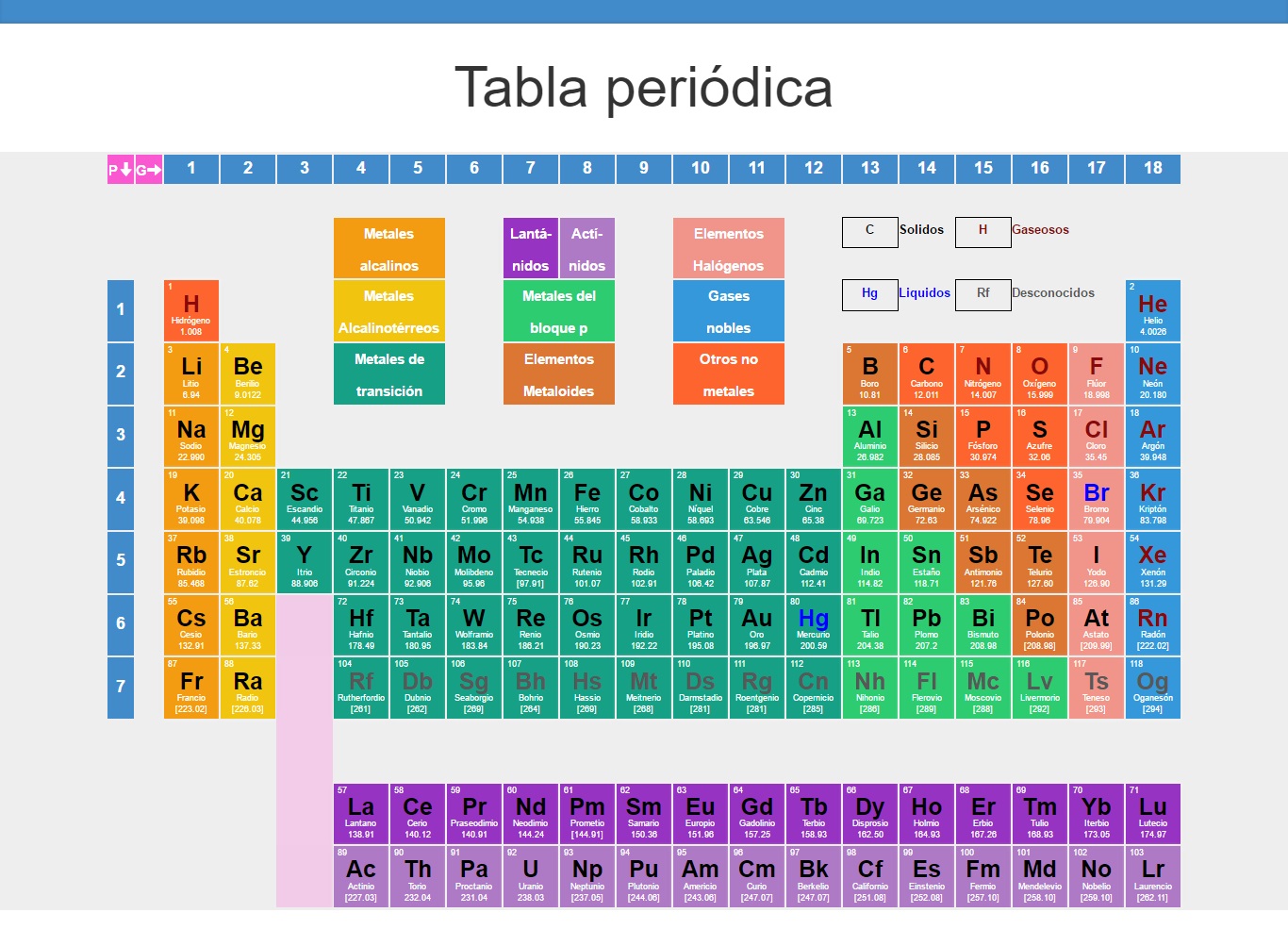
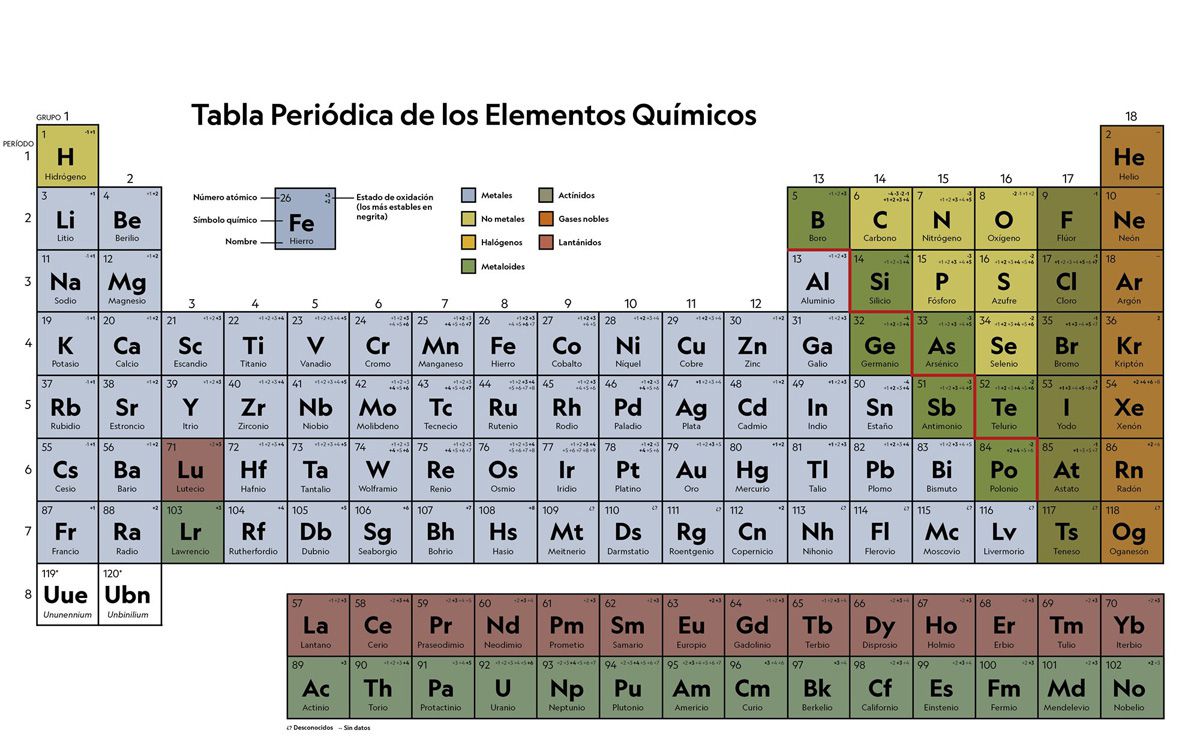
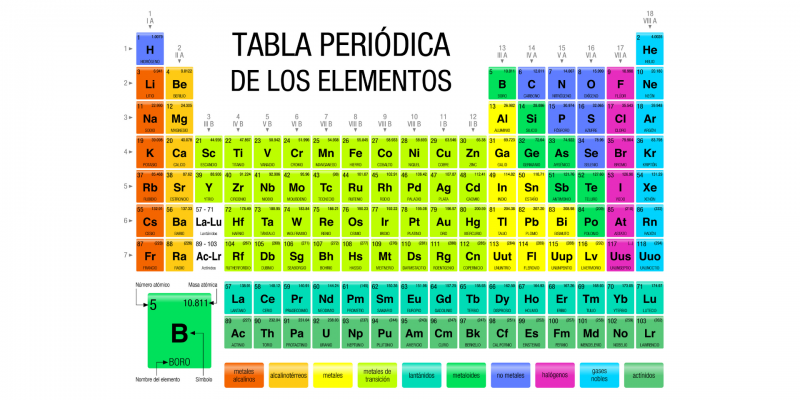
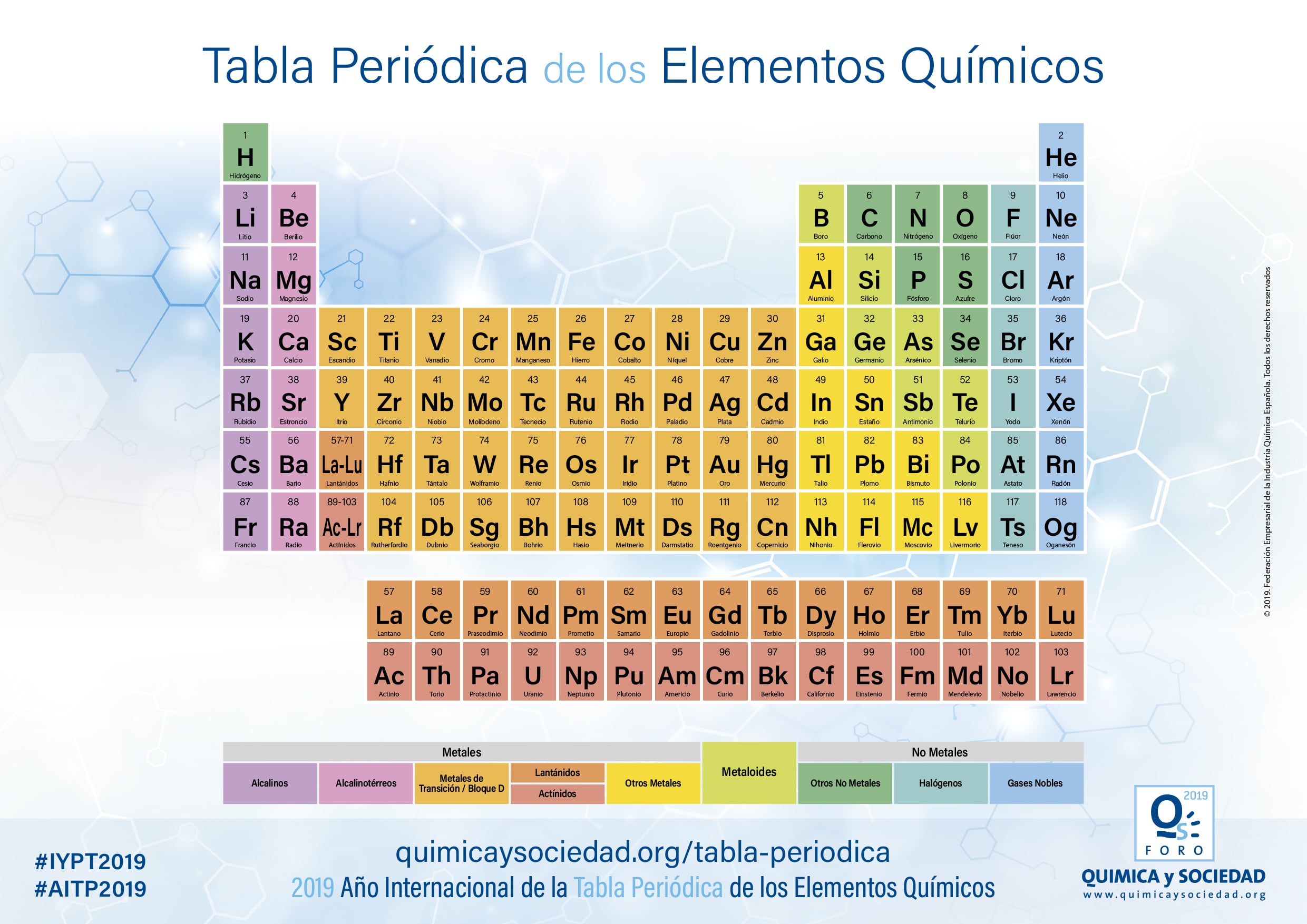
La tabla periódica es la herramienta principal para comprender la organización y las relaciones entre los elementos. Introduzcamos la tabla periódica de manera gradual. No es necesario abrumar a los estudiantes con todos los detalles a la vez. Comienza por explicar las filas (períodos) y las columnas (grupos o familias). Cada grupo comparte propiedades químicas similares.
Cada elemento en la tabla periódica está representado por un símbolo. El símbolo proviene de su nombre en latín, griego o inglés. H es para hidrógeno. O es para oxígeno. Fe es para hierro (Ferrum en latín). Entender el significado del símbolo ayuda a recordar y reconocer el elemento.
Los elementos se clasifican en metales, no metales y metaloides. Los metales son buenos conductores del calor y la electricidad. Los no metales son malos conductores. Los metaloides tienen propiedades intermedias. Esta clasificación básica facilita la comprensión de las propiedades generales de los elementos.
Relaciones Entre Elementos: Enlace Químico
Ahora, abordemos cómo se relacionan los elementos. La principal forma en que los elementos interactúan es a través del enlace químico. Los elementos se combinan para formar compuestos. El enlace químico ocurre porque los átomos buscan la estabilidad electrónica.
Hay dos tipos principales de enlace químico: enlace iónico y enlace covalente. En el enlace iónico, los electrones se transfieren de un átomo a otro. En el enlace covalente, los electrones se comparten entre los átomos. El agua (H2O) es un ejemplo de un compuesto con enlaces covalentes. La sal (NaCl) es un ejemplo de un compuesto con enlaces iónicos.
Expliquemos la regla del octeto. Los átomos tienden a ganar, perder o compartir electrones para lograr una configuración electrónica estable con ocho electrones en su capa de valencia (la capa más externa). Esto ayuda a entender por qué se forman ciertos enlaces y no otros.
Errores Comunes y Cómo Abordarlos
Un error común es pensar que los elementos son sustancias raras o exóticas. Enfatiza que los elementos están presentes en todo lo que nos rodea. Otro error es confundir elementos con compuestos. Aclara que los compuestos están formados por la combinación de dos o más elementos.
Algunos estudiantes creen que los elementos son inalterables. Explica que los elementos pueden transformarse en otros elementos a través de reacciones nucleares, pero esto es diferente a las reacciones químicas ordinarias. La radiactividad es un ejemplo de transformación nuclear.
Haciendo el Aprendizaje Atractivo
Incorpora actividades prácticas. Construir modelos de átomos con diferentes protones, neutrones y electrones ayuda a visualizar la estructura atómica. Utiliza la tabla periódica para predecir las propiedades de los elementos. Realizar experimentos sencillos, como la reacción de un metal con un ácido, demuestra las propiedades químicas de los elementos.
Utiliza analogías y metáforas. Compara la tabla periódica con un mapa que organiza los elementos. Compara el enlace químico con una danza en la que los átomos se unen para formar nuevas estructuras. Integra juegos y rompecabezas. Los crucigramas y los juegos de memoria con símbolos y nombres de elementos son herramientas útiles.
Fomenta la investigación. Asigna proyectos de investigación sobre elementos específicos y sus usos en la vida cotidiana. Invita a científicos o ingenieros a dar charlas sobre cómo utilizan los elementos en sus trabajos. Conecta el aprendizaje con el mundo real. Demuestra cómo el conocimiento de los elementos es importante para la medicina, la tecnología y la sostenibilidad.