Metales Alcalinotérreos En La Tabla Periodica

Queridos colegas,
Hoy exploraremos los metales alcalinotérreos. Un grupo fascinante de elementos en la tabla periódica.
¿Qué son los Metales Alcalinotérreos?
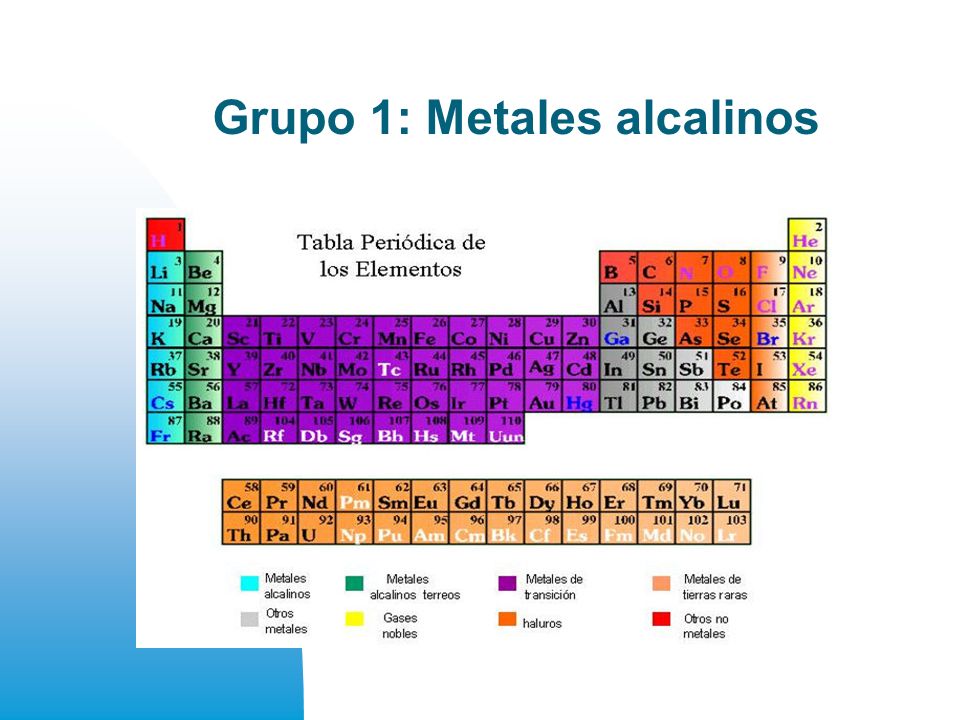
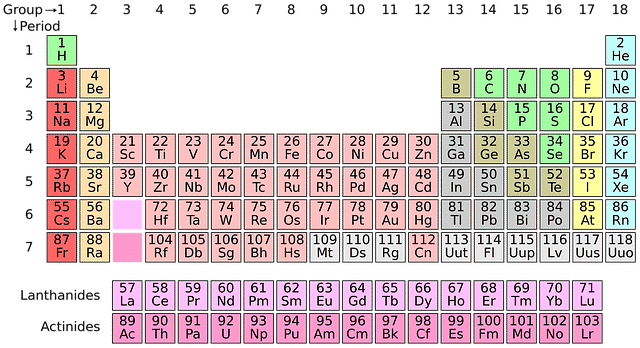
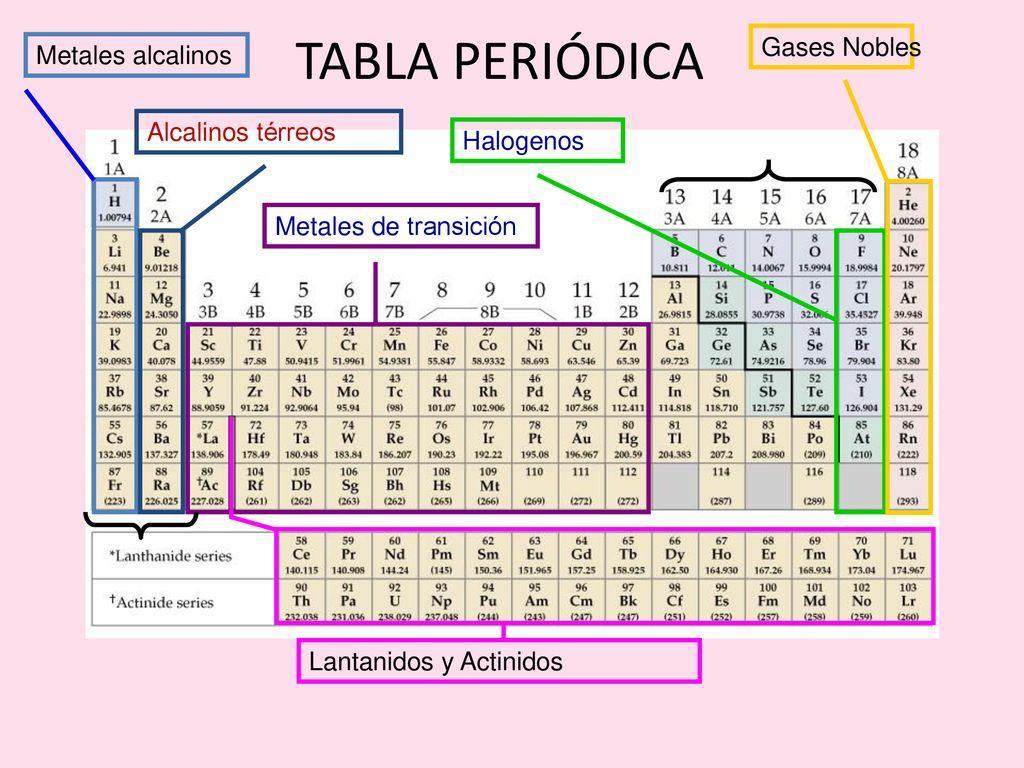
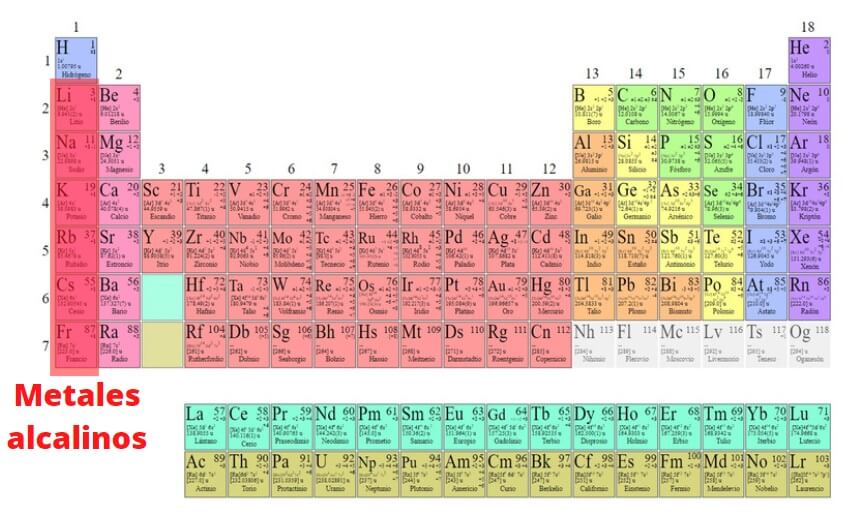
Los metales alcalinotérreos conforman el Grupo 2 de la tabla periódica. Incluyen elementos como el berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra). Todos comparten ciertas propiedades físicas y químicas.
Son metales brillantes, plateados-blancos. Son menos densos y duros que otros metales de transición. Son buenos conductores de electricidad, aunque no tan buenos como los metales alcalinos.
¿Cómo Explicar Esto en Clase?
Comiencen resaltando la posición en la tabla periódica. Muestren cómo el Grupo 2 está justo al lado del Grupo 1 (los metales alcalinos). Comparen sus reactividades relativas.
Usen ejemplos cotidianos. El magnesio en suplementos alimenticios. El calcio en productos lácteos. El bario en algunos estudios de rayos X.
Pueden demostrar la reactividad con agua. El calcio reacciona visiblemente con el agua. El magnesio requiere agua caliente o vapor.
Propiedades Clave
Los metales alcalinotérreos tienen dos electrones de valencia. Esto significa que tienden a perder estos dos electrones al reaccionar. Forman iones con una carga de +2.
Son reactivos, pero menos que los metales alcalinos. La razón es que tienen dos electrones de valencia que deben perder para alcanzar una configuración electrónica estable. Esto requiere más energía.
Su reactividad aumenta al bajar en el grupo. El radio es el más reactivo del grupo. Debido a que pierde sus electrones con mayor facilidad.
Errores Comunes
Es común que los estudiantes confundan a los metales alcalinotérreos con los metales alcalinos. Asegúrense de enfatizar la diferencia en reactividad.
Otro error es pensar que todos los metales son igualmente reactivos. Expliquen cómo la configuración electrónica y la carga nuclear afectan la reactividad.
Algunos estudiantes pueden creer que todos los metales alcalinotérreos son peligrosos. Si bien algunos compuestos pueden ser tóxicos, muchos son esenciales para la vida.
Haciendo el Concepto Atractivo
Realicen experimentos seguros y controlados. La reacción del calcio con agua. La llama coloreada que producen al quemar diferentes sales de metales alcalinotérreos.
Utilicen analogías. Comparen la pérdida de electrones con "dar" algo a otra persona. Cuanto más fácil sea "dar", más reactivo es el metal.
Incorporen la historia. Investiguen el descubrimiento de estos elementos. Las aplicaciones en la industria y la medicina.
Pueden usar simulaciones interactivas. Permiten a los estudiantes explorar las propiedades de los elementos. Experimentar con diferentes reacciones virtuales.
Aplicaciones Importantes
El magnesio se usa en aleaciones ligeras. El calcio es esencial para huesos y dientes. El bario se usa en radiología. El estroncio da el color rojo brillante a los fuegos artificiales.
Finalmente, recuerden que la tabla periódica es una herramienta poderosa. Ayuda a comprender las propiedades y el comportamiento de los elementos. Los metales alcalinotérreos son un excelente ejemplo de cómo las tendencias periódicas funcionan.
Espero que estas sugerencias les sean útiles. ¡Mucho éxito enseñando sobre los metales alcalinotérreos!