Tabla Periodica De Los Elementos Masa Atomica

¡Hola a todos! Preparémonos para dominar la Tabla Periódica y la Masa Atómica. No te preocupes, ¡lo haremos paso a paso! ¡Vamos a ello!
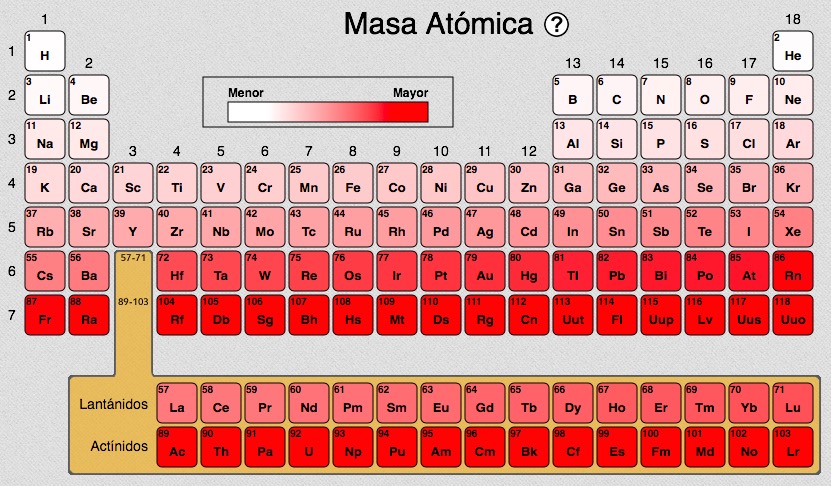
¿Qué es la Tabla Periódica?
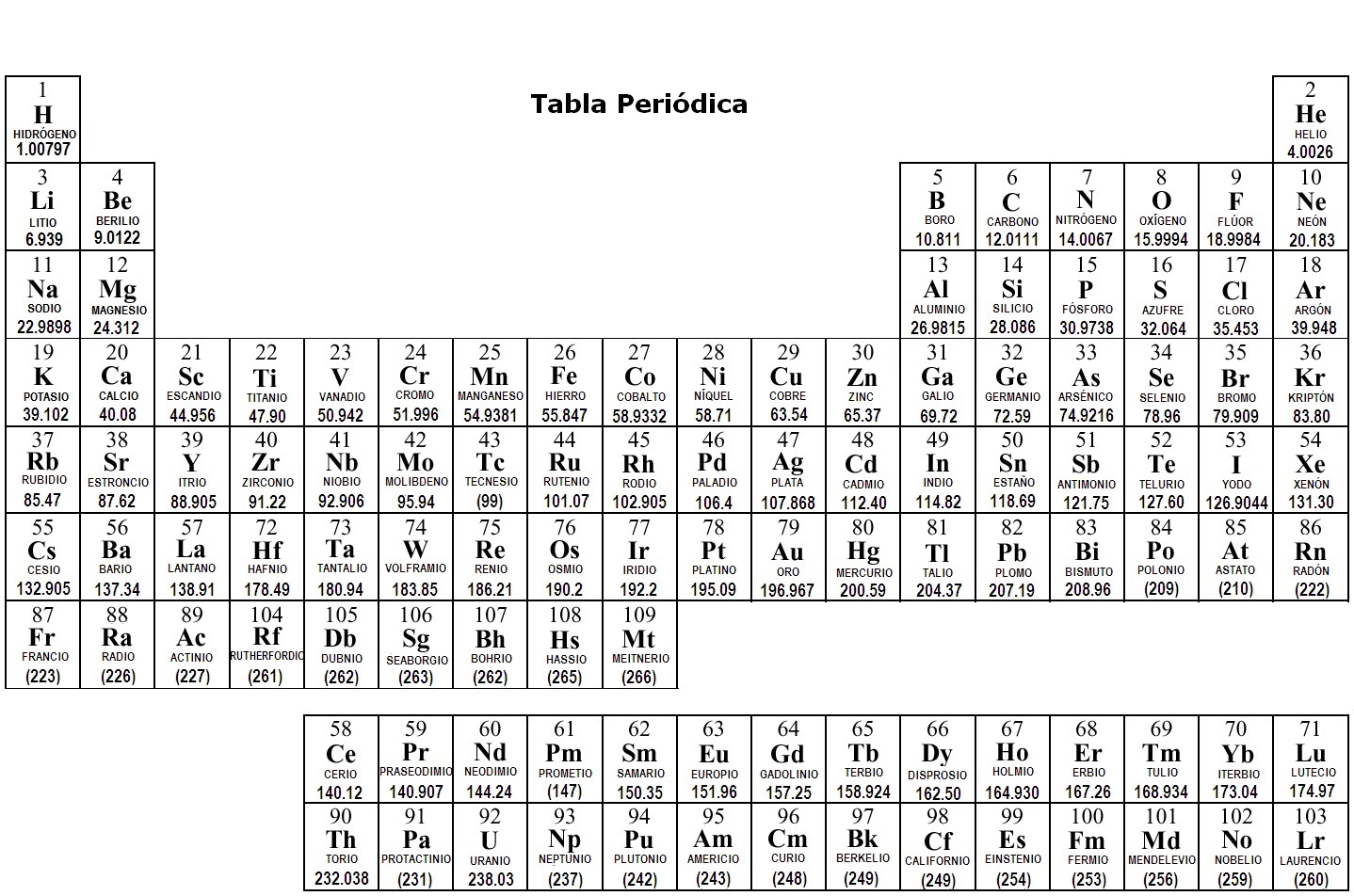
La Tabla Periódica es como un mapa de todos los elementos químicos conocidos. Organiza los elementos según sus propiedades. Cada elemento tiene su propio cuadro en la tabla.
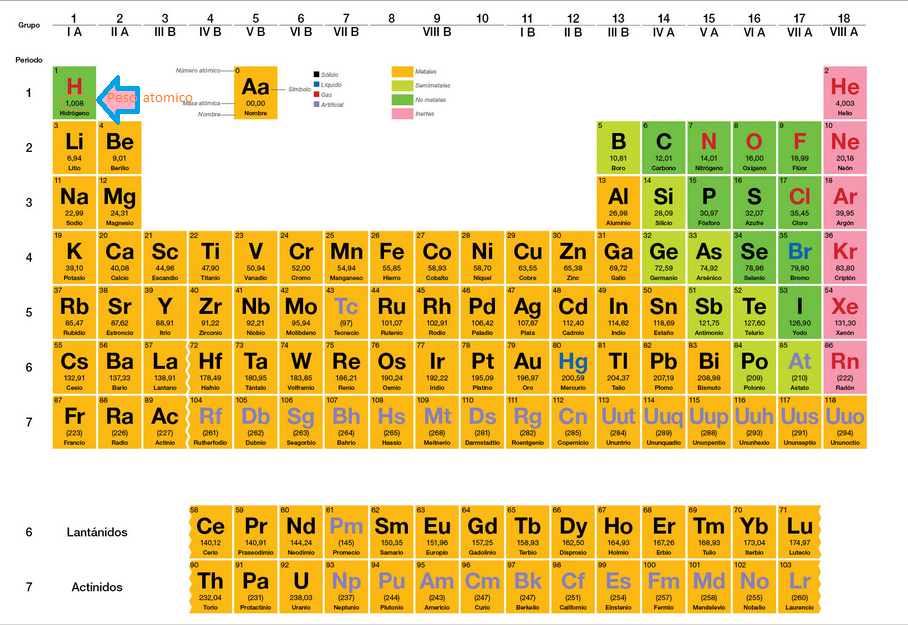
Cada cuadro contiene información importante sobre el elemento. Incluye el símbolo químico, el número atómico, y la masa atómica. ¡Estos datos son cruciales!
Entendiendo el Número Atómico
El número atómico es el número de protones que tiene un átomo de ese elemento. Es lo que define a un elemento. El número atómico es único para cada elemento.
Por ejemplo, el hidrógeno (H) tiene un número atómico de 1. Esto significa que cada átomo de hidrógeno tiene un protón. El oxígeno (O) tiene un número atómico de 8, lo que significa que tiene ocho protones.
¿Qué es la Masa Atómica?
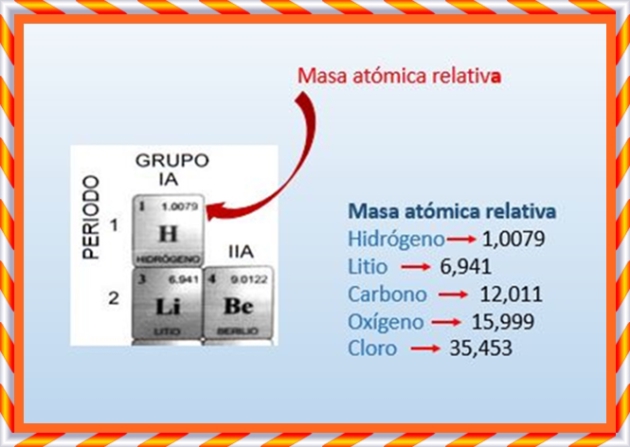
La masa atómica es la masa promedio de un átomo de un elemento. Se mide en unidades de masa atómica (uma). La masa atómica es una medida relativa, comparada con la masa del isótopo Carbono-12.
La masa atómica se encuentra generalmente debajo del símbolo del elemento en la Tabla Periódica. Es importante recordar que es un promedio. Tiene en cuenta los diferentes isótopos del elemento.
Isótopos y la Masa Atómica
Los isótopos son átomos del mismo elemento con diferente número de neutrones. Esto significa que tienen diferente masa. La masa atómica promedio considera la abundancia de cada isótopo.
Por ejemplo, el carbono tiene isótopos como el Carbono-12, Carbono-13, y Carbono-14. El Carbono-12 es el más abundante. La masa atómica del carbono es cercana a 12 uma, pero no exactamente, porque considera los otros isótopos.
Calculando la Masa Atómica Promedio
Para calcular la masa atómica promedio, necesitas conocer la masa de cada isótopo. También necesitas conocer su abundancia relativa. Multiplica la masa de cada isótopo por su abundancia. Luego suma los resultados.
Por ejemplo, si un elemento tiene dos isótopos: Isótopo A (masa = 10 uma, abundancia = 50%) e Isótopo B (masa = 12 uma, abundancia = 50%). La masa atómica promedio seria (10 * 0.50) + (12 * 0.50) = 11 uma.
Usando la Tabla Periódica para Encontrar la Masa Atómica
La Tabla Periódica es tu mejor amiga para encontrar la masa atómica. Simplemente busca el elemento que necesitas. Localiza el número que se encuentra generalmente debajo del símbolo del elemento. ¡Ese es la masa atómica!
Recuerda que la masa atómica es un valor promedio. Es una herramienta valiosa para cálculos químicos. Siempre verifica las unidades (uma).
Importancia de la Masa Atómica
La masa atómica es crucial para la estequiometría. La estequiometría es el estudio de las relaciones cuantitativas entre los reactivos y los productos en una reacción química. Permite calcular las cantidades de sustancias involucradas en una reacción.
También es importante para entender las propiedades químicas de los elementos. La masa atómica, junto con la configuración electrónica, influye en cómo un elemento reacciona con otros elementos. Estos datos te permitirán predecir el comportamiento de los elementos.
Resumen
¡Felicidades, has llegado al final! Recuerda que la Tabla Periódica organiza los elementos. El número atómico define el elemento. La masa atómica es el promedio de las masas de los isótopos. ¡Usa esta información para conquistar tus exámenes! ¡Tu puedes!