Gilbert Newton Lewis Aportaciones Ala Quimica

Analizar y resolver el problema de las aportaciones de Gilbert Newton Lewis a la química requiere un enfoque metódico. Empezamos examinando las fuentes disponibles. Identificamos sus contribuciones más significativas.
Primero, recopilamos información sobre Lewis. Consultamos libros de texto, artículos científicos y recursos en línea confiables. Buscamos información biográfica y detalles sobre su trabajo experimental y teórico.
Luego, analizamos la información recopilada. Buscamos patrones y temas recurrentes. Intentamos comprender el contexto histórico en el que Lewis realizó su trabajo.
Ahora, evaluamos la importancia de sus aportaciones. ¿Cómo influyeron sus ideas en el desarrollo de la química? ¿Qué problemas resolvieron sus teorías?
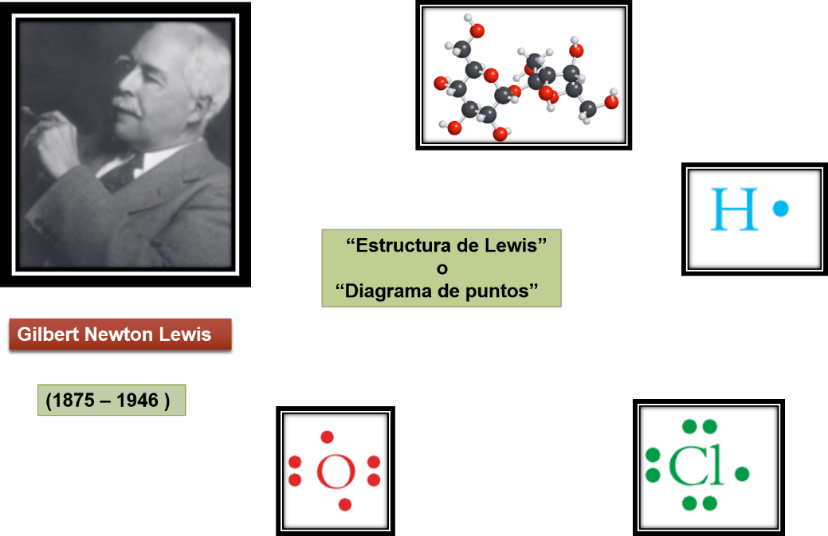
El Enlace Covalente y la Regla del Octeto
Una de las contribuciones más importantes de Lewis es su teoría del enlace covalente. Propuso que los átomos comparten electrones para formar enlaces químicos. Esta idea revolucionó la comprensión de la estructura molecular.
La regla del octeto es otra de sus ideas clave. Establece que los átomos tienden a ganar, perder o compartir electrones para alcanzar una configuración electrónica estable con ocho electrones en su capa de valencia. Esto simplificó la predicción de la estabilidad de muchas moléculas.
Sin embargo, la regla del octeto tiene sus limitaciones. No se aplica a todas las moléculas, especialmente a aquellas con un número impar de electrones o átomos con más de ocho electrones en su capa de valencia. Es importante reconocer estas excepciones.
Termodinámica y la Escala de Acidez de Lewis
Lewis también realizó contribuciones significativas a la termodinámica. Estudió la energía libre y la entalpía de las reacciones químicas. Su trabajo ayudó a establecer las bases de la termodinámica química moderna.
Desarrolló la escala de acidez de Lewis. Esta escala define los ácidos como aceptores de pares de electrones y las bases como donadores de pares de electrones. Amplió la definición tradicional de ácidos y bases.
Esta definición es más general que la definición de Brønsted-Lowry. Permite clasificar como ácidos y bases a compuestos que no contienen protones. Consideramos las implicaciones de esta definición más amplia.
Análisis Crítico y Síntesis
Es importante analizar críticamente las ideas de Lewis. Identificamos las fortalezas y debilidades de sus teorías. Consideramos las críticas que recibió su trabajo.
Por ejemplo, su teoría del enlace covalente fue posteriormente refinada por la mecánica cuántica. La mecánica cuántica proporcionó una descripción más precisa de la distribución electrónica en las moléculas. Aun así, la teoría de Lewis sigue siendo una herramienta útil para comprender la estructura molecular básica.
Finalmente, sintetizamos la información recopilada y analizada. Elaboramos una evaluación completa de las aportaciones de Gilbert Newton Lewis a la química. Presentamos nuestras conclusiones de manera clara y concisa.
Recordamos que Lewis no siempre recibió el reconocimiento que merecía durante su vida. Algunos de sus descubrimientos fueron atribuidos a otros científicos. Es importante reconocer su contribución única al campo de la química.
Las ideas de Lewis siguen siendo relevantes en la química moderna. Sus teorías sobre el enlace covalente, la regla del octeto y la termodinámica son fundamentales para la comprensión de la química. Estudiar su trabajo es esencial para cualquier estudiante de química.